大学院|岐阜大学医学部附属病院 循環器内科・腎臓内科

- 人材育成
- 大学院
大学院医学系研究科(博士課程)の案内
岐阜大学大学院研究科(循環器内科学・呼吸器内科学・腎臓内科学)では、各分野での基礎研究・臨床研究・トランスレーショナル研究を行う大学院生を募集します。
医学生・初期研修医から後期研修医、若手・中堅医師のみなさまを始め、更なるキャリアアップを望まれる方は、是非一度気軽にご相談ください。
また本教室では、社会人大学院生も受け入れており、豊富な実績を有しています。岐阜大学医学部附属病院以外の病院に勤務する医師・メディカルスタッフの募集も積極的にしています。
- 循環器内科学研究分野は、心筋梗塞、心不全や不整脈に加え、高血圧、糖尿病、脂質異常症、肥満といった生活習慣病など疾患が非常に多岐にわたります。 これらの疾患に対して包括的に臨床研究・基礎研究を行っています。また工学部チームや企業等との共同研究も実施しています。詳細は下記を参照ください。
- 腎臓内科分野では、急性・慢性腎不全,各種腎炎,ネフローゼ症候群などの腎臓疾患・透析治療について診療を行っております。 現在まで行った研究では”血液透析患者における左室拡張機能不全に対する長期レボカルニチン投与の改善効果”や”医薬品副作用自発報告データベース(JADER)によるリアルワールドデータを用いたボノプラザン誘発腎障害の解析”等について研究を行い、成果発表しております。 現在進行している研究では、”維持透析患者における心血管病変の進展及び抑制に関与する因子の検討”、などがあります。 進学を希望される先生方のご連絡をお待ちしています。
医学系研究科 | 国立大学法人東海国立大学機構 岐阜大学
大学院のシラバスをご入用の方は問い合わせフォームにてお申し付けください。
循環器内科分野
基礎研究グループ
1. 心筋梗塞後心不全に対する我々の取り組み
現在の急性心筋梗塞治療として、急性期の冠動脈形成術による冠動脈再灌流や各種薬剤による心臓リモデリング抑制、心機能保持が期待されますが、心機能低下例においては現存治療に限界があります。 当教室では従来とは異なる治療法を開発、研究しております。今までに動物実験で心筋梗塞後にサイトカインのG-CSF、エリスロポエチン投与が梗塞心筋組織を修復・再生し左室リモデリングを改善、心機能を改善することを報告してきました。 また、再生医療の細胞治療として、間葉系幹細胞のMuse細胞を用いて、心筋梗塞後の心機能保護効果があることも報告しました。
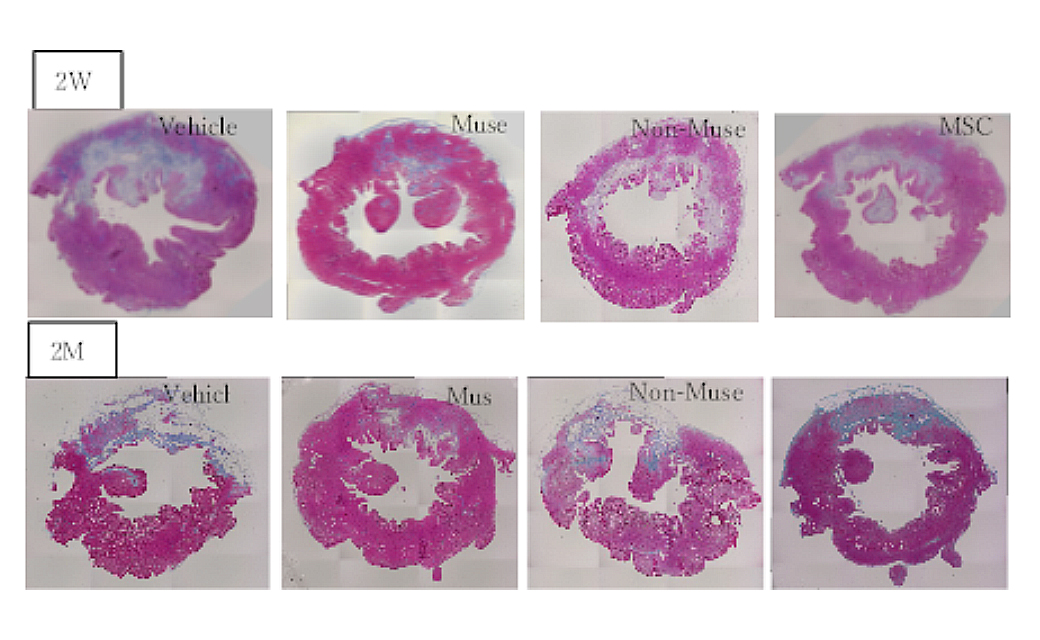 ウサギ心筋梗塞後の心臓短軸スライスMasson trichrome染色(論文3)
ウサギ心筋梗塞後の心臓短軸スライスMasson trichrome染色(論文3)
- 1. Postinfarct active cardiac-targeted delivery of erythropoietin by liposomes with sialyl Lewis X repairs infarcted myocardium in rabbits.
Yamada Y, Kobayashi H, Minatoguchi S et al. Am J Physiol Heart Circ Physiol 2013; 304: H1124-H1133 - 2. Post-MI treatment with G-CSF and EPO-liposome with SLX repairs infarcted myocardium through EPCs mobilization and activation of prosurvival signals in rabbits.
Yamada Y, Minatoguchi S, Minatoguchi S et al. Pharmacol Res Perspect.: 2018; 7(1): e00451 - 3. S1P-S1PR2 Axis Mediates Homing of Muse Cells Into Damaged Heart for Long-Lasting Tissue Repair and Functional Recovery After Acute Myocardial Infarction.
Yamada Y, Wakao S, Minatoguchi S et al. Circulation Research: 2018; 122: 1069-1083 - 4. Mobilized Muse Cells After Acute Myocardial Infarction Predict Function and Remodeling in the Chronic Phase.
Tanaka T, Nishigaki K, Minatoguchi S et al. Circ J. 2018 Jan 25;82(2):561-571 - 5. lHuman Muse cells reduce myocardial infarct size and improve cardiac function without causing arrythmias in a swine model of acute myocardial infarction
Yamada Y, Minatoguchi S, Minatoguchi S et al. PLos One. 2022 Mar 24; 17(3): e0265347
- ESC congress 2015 (London, UK) 2015.8.29-9.2
- 1. Yoshihisa Yamada, Shingo Minatoguchi, Hiromitsu Kanamori, Kenshi Higashi, Masanori Kawasaki, Kazuhiko Nishigaki, Atsushi Mikami, Shohei Wakao, Mari Dezawa, Shinya Minatoguchi
Sphigosine-mono-phosphate (S1P) induces the migration of Muse cells but not non-Muse cells toward the rabbit post-infarct heart and contributes to the improvement of cardiac function and remodeling - AHA Scientific session 2015 (Orland, Florida, USA) 2015, 11.7-11.11
- 1. Yoshihisa Yamada, Shingo Minatoguchi, Hiromitsu Kanamori, Kenshi Higashi, Masanori Kawasaki, Kazuhiko Nishigaki, Atsushi Mikami, Shohei Wakao, Mari Dezawa, Shinya Minatoguchi
Post-infarct administration of Multilineage-differentiating stress enduring (Muse) cells regenerates cardiomyocytes and microvessels and improves cardiac function and remodeling in rabbits - 第63回日本心臓病学会学術集会(横浜)2015,9.18-9.20
- 1. Yoshihisa Yamada, Shingo Minatoguchi, Hiromitsu Kanamori, Kenshi Higashi, Masanori Kawasaki, Kazuhiko Nishigaki, Atsushi Mikami, Shohei Wakao, Mari Dezawa, Shinya Minatoguchi
Muse細胞による急性心筋梗塞の治療(シンポジウム発表) - ESC congress 2016 (Rome, Italy) 2016, 8.27-8.31
- 2. Yoshihisa Yamada, Shingo Minatoguchi, Shinya Baba, Sanae Shibata, Satoshi Takashima, Hiromitsu Kanamori, Masanori Kawasaki, Kazuhiko Nishigaki, Atsushi Mikami, Shohei Wakao, Mari Dezawa, Shinya Minatoguchi
Human xenograft Muse cells reduce the myocardial infarct size and improve the cardiac function and remodeling in a miniature pig model of acute myocardial infarction (Rapid Fire Abstract) - 第16回日本再生医療学会総会 (仙台2017. 3.7-9)
- Yoshihisa Yamada, Masamitsu Iwasa, Hiroaki Ushikoshi, Kazuhiko Nishigaki, Shinya Minatoguchi
G-CSFとSLX結合エリスロポエチン内包リポソームによる虚血心筋保護効果 - AHA Scientific session 2018 (Chicago, IL, USA) 2018, 11.10-11.12
- 1. Yoshihisa Yamada, Shingo Minatoguchi, Shinya Baba, Sanae Shibata, Satoshi Takashima, Masanori Kawasaki, Atsushi Mikami, Shohei Wakao, Mari Dezawa, Shinya Minatoguchi
Post-infarct administration of human xenograft Muse cells reduce the myocardial infarct size and improve the cardiac function and remodeling in a miniature pig model
2. 細胞死、オートファジーに着目した心不全へのアプローチ
心不全の原因は虚血性心疾患や心筋症など様々ですが代償期を経て最終的に心機能不全(心不全)に陥ります。 近年では高齢化に伴い“心不全パンデミック”が叫ばれ世界的に問題となっています。 心不全に対する治療はデバイスや薬物治療の進歩により一定の効果を上げてきましたがまだまだ十分とは言えません。
我々の研究室ではこの心不全をテーマに研究しています。高血圧、糖尿病、心筋梗塞、慢性腎臓病、心筋症など種々の疾患の動物モデルを用いて心不全の発症メカニズム、新しい治療法の開発を模索しています。 特に臨床現場から得られた心筋生検の病理像は大切であり、例えばそこでみられる細胞死やオートファジーに関する形態変化は大きなヒントになります。 2016年に大隅良典博士がノーベル賞を受賞され、一躍注目を浴びたオートファジーに関する研究は当教室でもその10年以上前から注目してきました。
我々は心筋オートファジーの役割を明らかにする中でオートファジーが心機能の維持に重要であり心不全治療のターゲットになり得ることを報告しました。
これらの研究成果は日本循環器学会をはじめとする国内主要学会、米国心臓協会学術集会(AHA)、ヨーロッパ心臓病学会(ESC)で報告を重ね、国際的な学術誌にも発表しています。
我々は動物実験を繰り返し心筋オートファジーの役割を明らかにする中で虚血心筋症、薬剤性心筋症、糖尿病心筋症、δサルコグリカン心筋症など個々の原疾患によりオートファジーの応答は異なるもののオートファジーが心機能の維持に重要であり心不全治療のターゲットになり得ることを報告しました。 この知見を発展させヒト心筋生検標本を用いた研究では拡張型心筋症心筋においてオートファジーの活性が高いほど左室リバースリモデリングに成功する確率が高く、リバースリモデリングにした症例はその後の生命予後が良いことを報告しました。
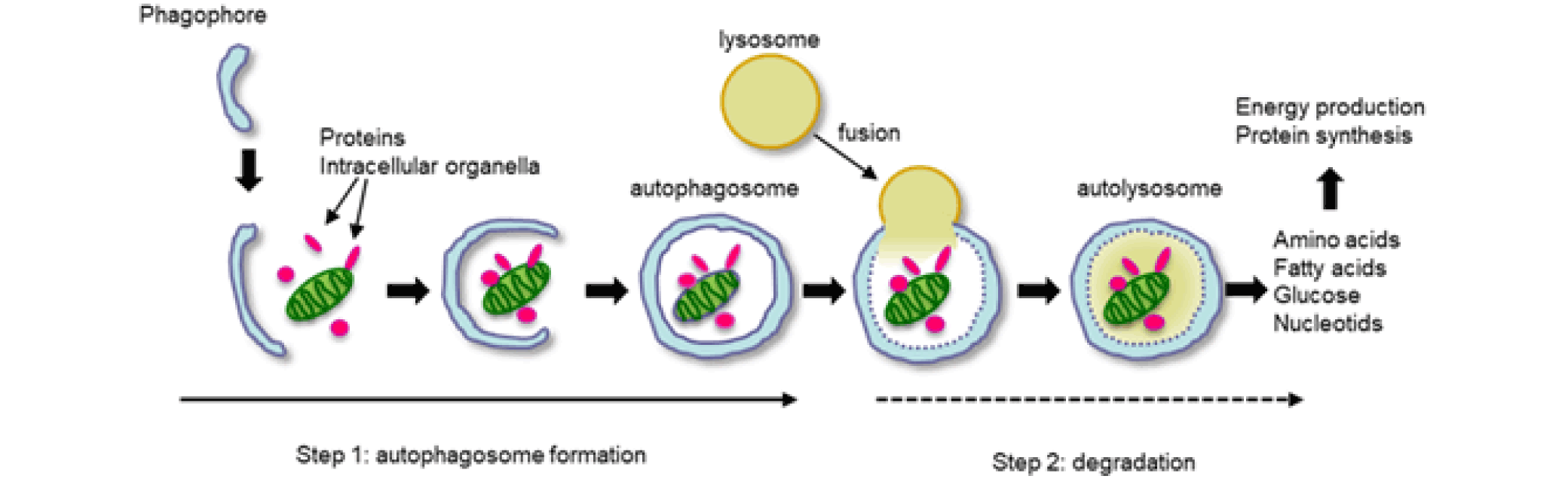 オートファジーのプロセス Kanamori H, et al. J Cardiol. 2021;77:30-40.
オートファジーのプロセス Kanamori H, et al. J Cardiol. 2021;77:30-40.
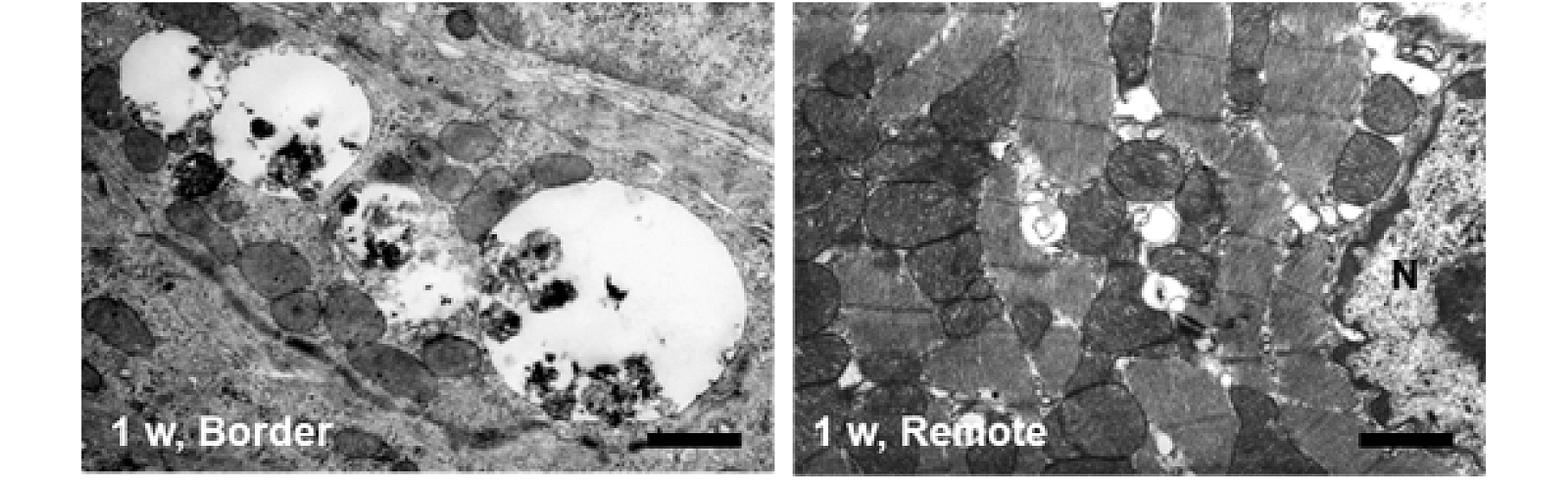 心筋梗塞後亜急性期のオートファジー空胞 Kanamori H, Cardiovasc Res. 2011;91:330-9.
心筋梗塞後亜急性期のオートファジー空胞 Kanamori H, Cardiovasc Res. 2011;91:330-9.
- 1. Kanamori H, Yoshida A, Naruse G,et al. Impact of Autophagy on Prognosis of Patients With Dilated Cardiomyopathy. J Am Coll Cardiol. 2022;79:789-801.
- 2. Kanamori H, Naruse G, Yoshida A, et al. Metformin Enhances Autophagy and Provides Cardioprotection in δ-Sarcoglycan Deficiency-Induced Dilated Cardiomyopathy. Circ Heart Fail. 2019;12:e005418.
- 3. Yoshida A, Kanamori H, Naruse G, et al. (Pro)renin Receptor Blockade Ameliorates Heart Failure Caused by Chronic Kidney Disease. J Card Fail. 2019;25:286-300.
- 4. Naruse G, Kanamori H, Yoshida A, et al. The intestine responds to heart failure by enhanced mitochondrial fusion through glucagon-like peptide-1 signalling. Cardiovasc Res. 2019;115:1873-1885.
- 1. Yoshida A, et al. (Pro)renin Receptor Blockade Ameliorates Renal Dysfunction-Associated Heart Failure by suppressing Cardiac Fibrosis but not by interfering with Autophagy. American Heart association SCIENTIFIC SESSION 2017 (Anaheim, USA) 2017,11.11-15
- 2. Kanamori H, et al. Metformin Displays Cardioprotection in δ-sarcoglycan Deficiency Induced Cardiomyopathy Through Autophagic Activation via AMPK-mTOR Pathway. American Heart Association SCIENTIFIC SESSION 2017 11.11-15 Anaheim, CA, USA
- 3. Naruse G, et al. Miglitol mitigates hypertensive cardiomyopathy by mitochondria restoration via glucagon-like peptide-1 receptor/PKA/Drp1 dependent signaling pathway. American Heart association SCIENTIFIC SESSION 2016 (New Orleans, LA, USA) 2016,11.12-16
臨床研究グループ
下記以外にも、臨床不整脈研究や虚血性心疾患、心筋症のレジストリ研究への登録事業等を行っております。大学院生のニーズに合わせて希望する研究テーマを選択することができます。 大学院進学を検討されている方は、問い合わせフォームよりご気軽に相談ください。
1. テレメトリー式生体信号測定装置を用いた心拍数測定等を指標とした心臓リハビリテーション運動指導による慢性期心疾患患者の運動耐容能改善効果の検討
心臓リハビリテーション(心リハ)の有用性について、これまでに多くのエビデンスが蓄積されています。
今日では、心臓リハビリテーションは心不全の病態の進行を抑制または軽減し、再発・再入院・死亡を減少させ、快適で活動的な生活を実現するために広く施行されています。
2018年に循環器病対策推進基本計画が閣議決定され、その中に循環器疾患に対するリハビリテーションの拡充も盛り込まれています。
本研究グループでは、歩数測定や脈拍を24時間連続測定することができる腕時計型のテレメトリー式生体信号測定ウェアラブルデバイスを用いて、慢性心疾患患者の活動量のレポートをします。
患者の運動強度や脈拍を客観的かつ視覚的に確認可能であり、定期診察の際などに医師や理学療法士、看護師からフィードバックを受けることが容易になることが考えられるでしょう。
自宅で運動前後の脈拍数、歩数等の情報による身体活動量、夜間睡眠時の心拍数、昼間の安静時心拍数の平均値や変動を明らかにすることができ、自宅における心拍数や活動度を非侵襲的かつ簡便に、さらに客観的に評価できるようになります。
その結果を外来時に適切に患者にフィードバックを行うことにより、患者が適切な運動強度での運動を行うことが可能となり、患者自身の運動に対するモチベーションの変化にも繋がることが想定され、結果として運動耐容能改善の一助となることが想定されると考えています。
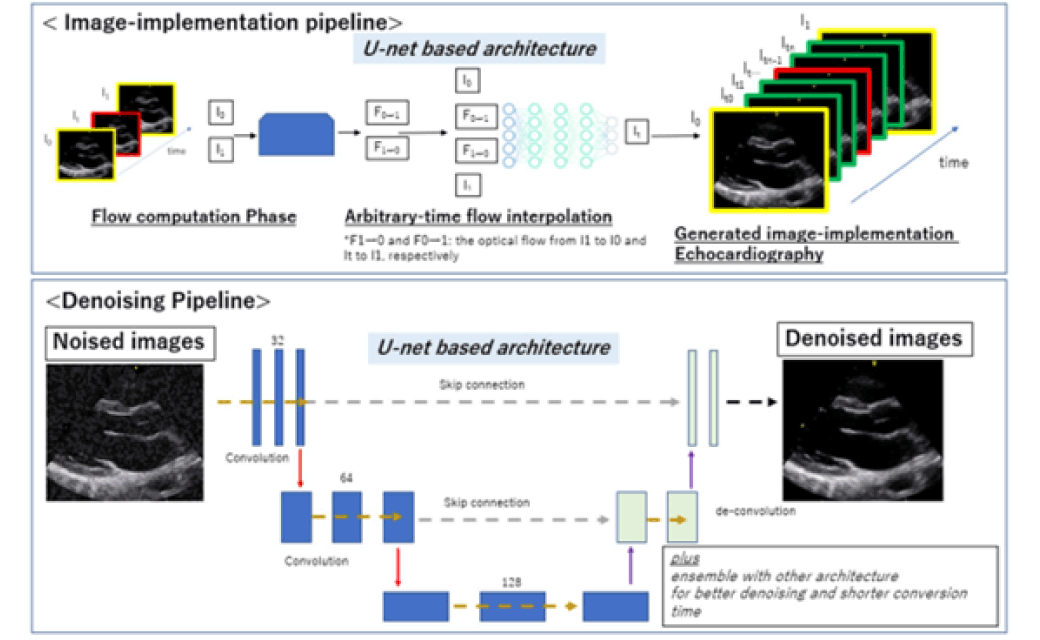
2. 人工知能を利用した心エコー機器の開発
近年、人工知能の心臓超音波領域への応用により、AIによるパラメータの自動解析や心疾患のフェノタイピングの同定が試みられています。 心エコー図検査はその非侵襲性や簡便性により、心疾患領域の日常臨床で汎用されていますが、一方で音響陰影アーチファクト やスペックルノイズによる超音波画質の低下により、臨床診断の正確性やパラメータ測定には一定の限界を伴っています。 ニューラルネットワークを用いた超音波画像のノイズリダクション処理、超音波画像間のオプティカルフローの推定による画像間自動補完を行うことを目的としています。 それにより超音波画質の向上および、心エコー図動画の平滑化処理を可能とし、画質向上技術(image super-resolution)が日常診断における診断精度の向上に寄与するかどうかを検討しています。
2019年に岐阜大学に人工知能研究推進センターが設立され医用工学研究の発展的拡大が計画され、これまでの共同研究の知見を経て、AIを用いた画像診断に関する研究を工学部と共同で行っています。
本研究は第86回日本循環器学会プレナリーセッションで発表を行いました。
腎臓内科分野
腎臓内科では関連病院の血液透析患者を対象に心血管病変の進展及び抑制に関与する因子の検討を行っています。
以前より透析患者では心臓弁膜症や心筋梗塞といった、心血管疾患の合併率が高いことが知られています。
原因としては体内のミネラル代謝異常や尿毒症物質、慢性炎症等の関与が指摘され、一方で近年はマグネシウムの血管石灰化の抑制効果が注目されています。
これら透析患者の心血管病変の進展や抑制に関与する因子を同定する事は、その治療方法や生命予後の改善に繋がると考えています。
方法としては透析条件や使用薬剤並びに定期的に行う検査(採血検査、生理検査(心臓超音波検査、足関節上腕血圧比)、 CT検査)のデータより心臓や血管の石灰化に関連している原因について調査・検討を行います。
これらの結果は適宜、関連学会で報告を行っております。
興味のある方はぜひご連絡ください。

