研究内容
N型糖鎖の枝分かれ構造の形成と機能についての研究
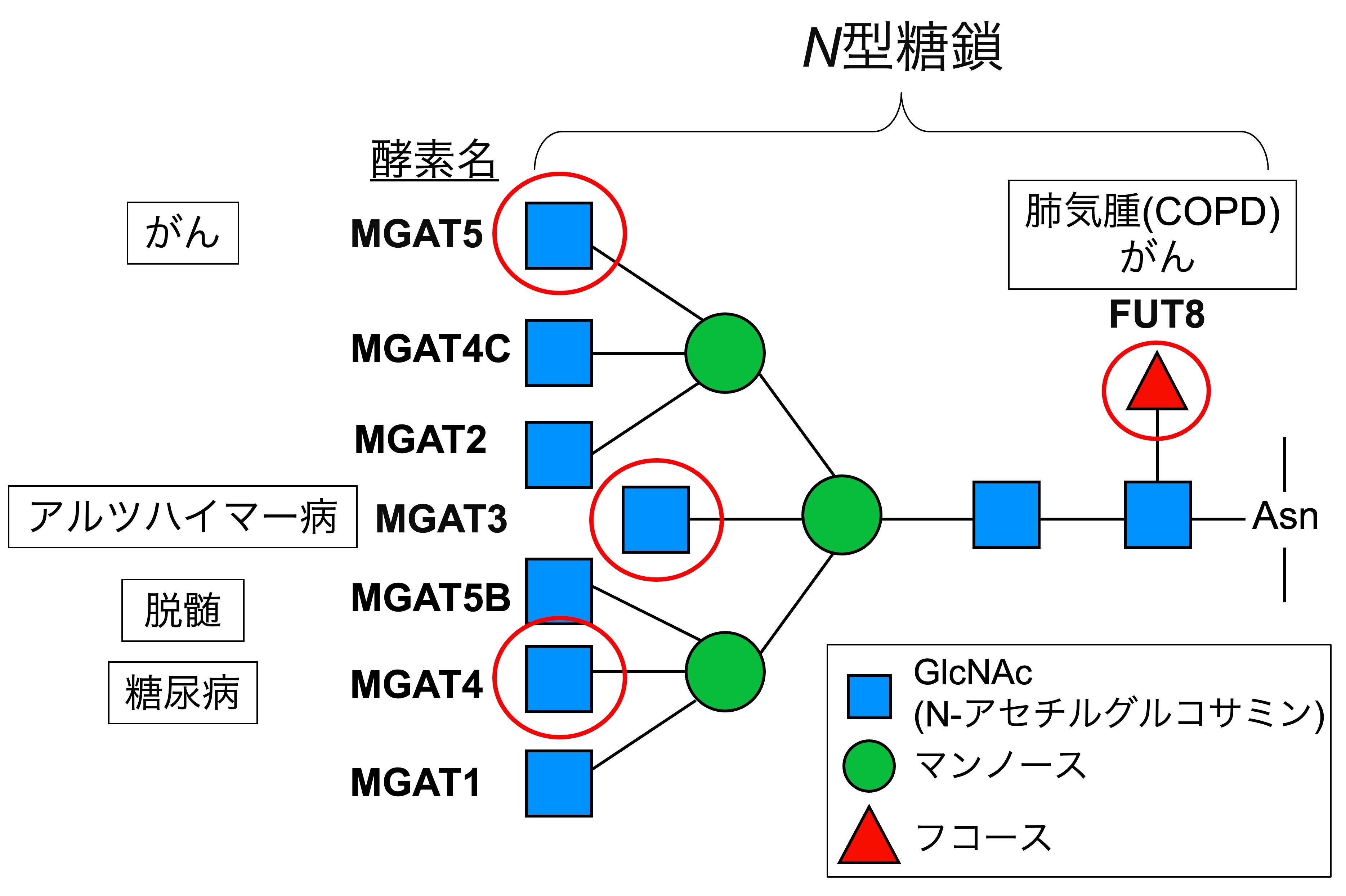
図1. N型糖鎖の枝分かれ構造と生合成酵素、疾患との関連性
当研究室では、タンパク質に結合したN型糖鎖の発現・機能・疾患との関わりを研究しています。中でも、糖鎖の枝分かれ構造に着目しています。
N型糖鎖は、タンパク質の普遍的な糖鎖修飾で、様々な構造のバリエーションを持っています。特に、2から5つ程度の枝分かれ構造があることが特徴です。それぞれの糖の枝には固有の機能があり、特定の疾患に関わることがわかってきています(図1)。さらに、それぞれの枝にはタンパク質選択性があり、特定の枝を持った糖鎖は限られたタンパク質にしかつきません。ところが、それぞれの糖鎖の枝が機能を発揮する分子メカニズムや、タンパク質選択性が生み出されるメカニズムについてはほとんどわかっていません。
当研究室では、枝分かれ構造の生合成を担う酵素(糖転移酵素)に着目して、これらの疑問に取り組んでいます。最終的には、これらの糖鎖が関連する疾患の治療につながることを目指しています。
アルツハイマー病を進行させるバイセクト糖鎖(bisecting GlcNAc)の研究
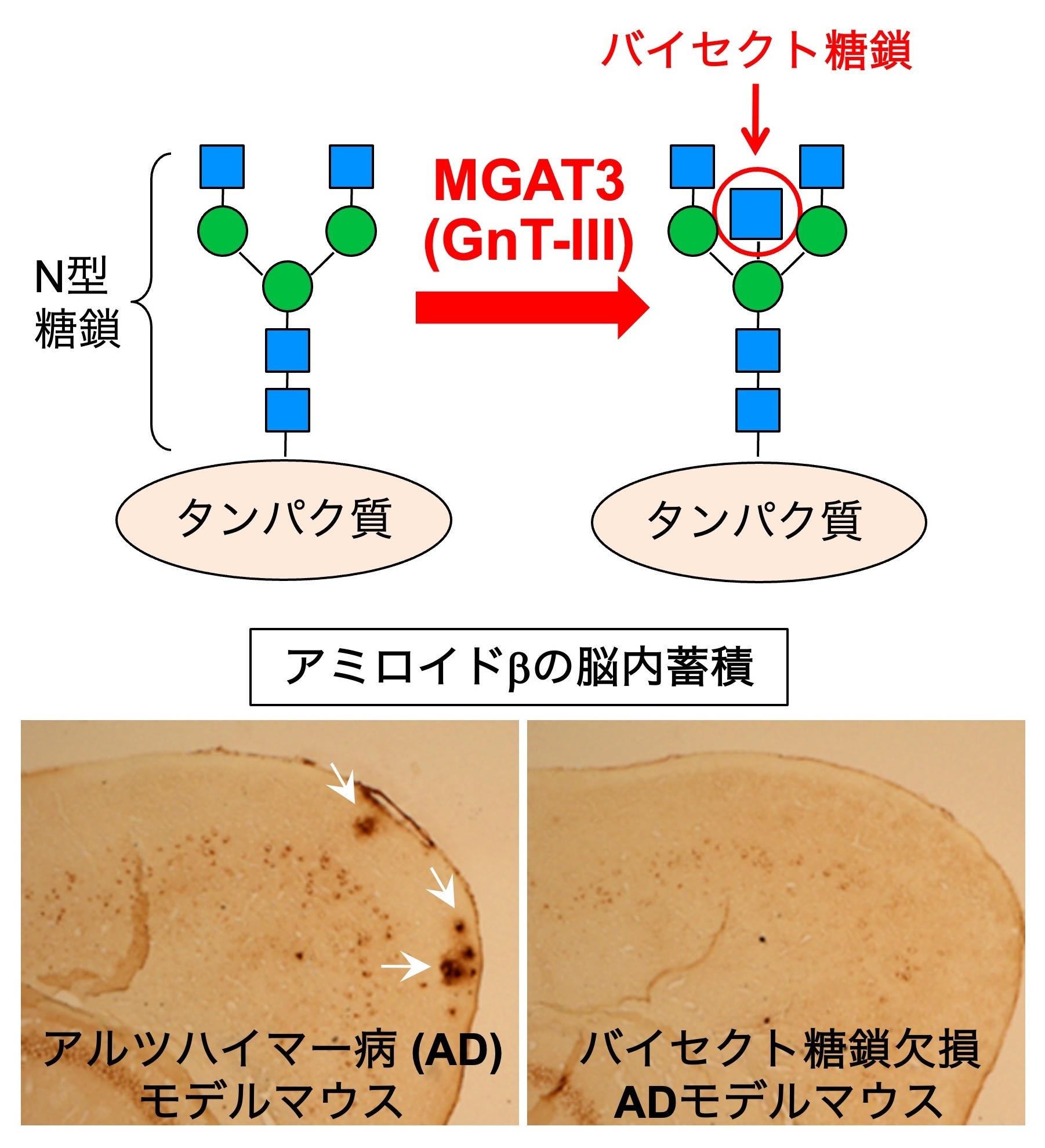
図2. (上) バイセクト糖鎖の構造と生合成酵素(下) アルツハイマー病のモデルマウスの脳に蓄積するアミロイドβ。バイセクト糖鎖欠損マウスではアミロイドβが激減する。
(参考文献:Kizuka et al., EMBO Mol. Med., 2015)
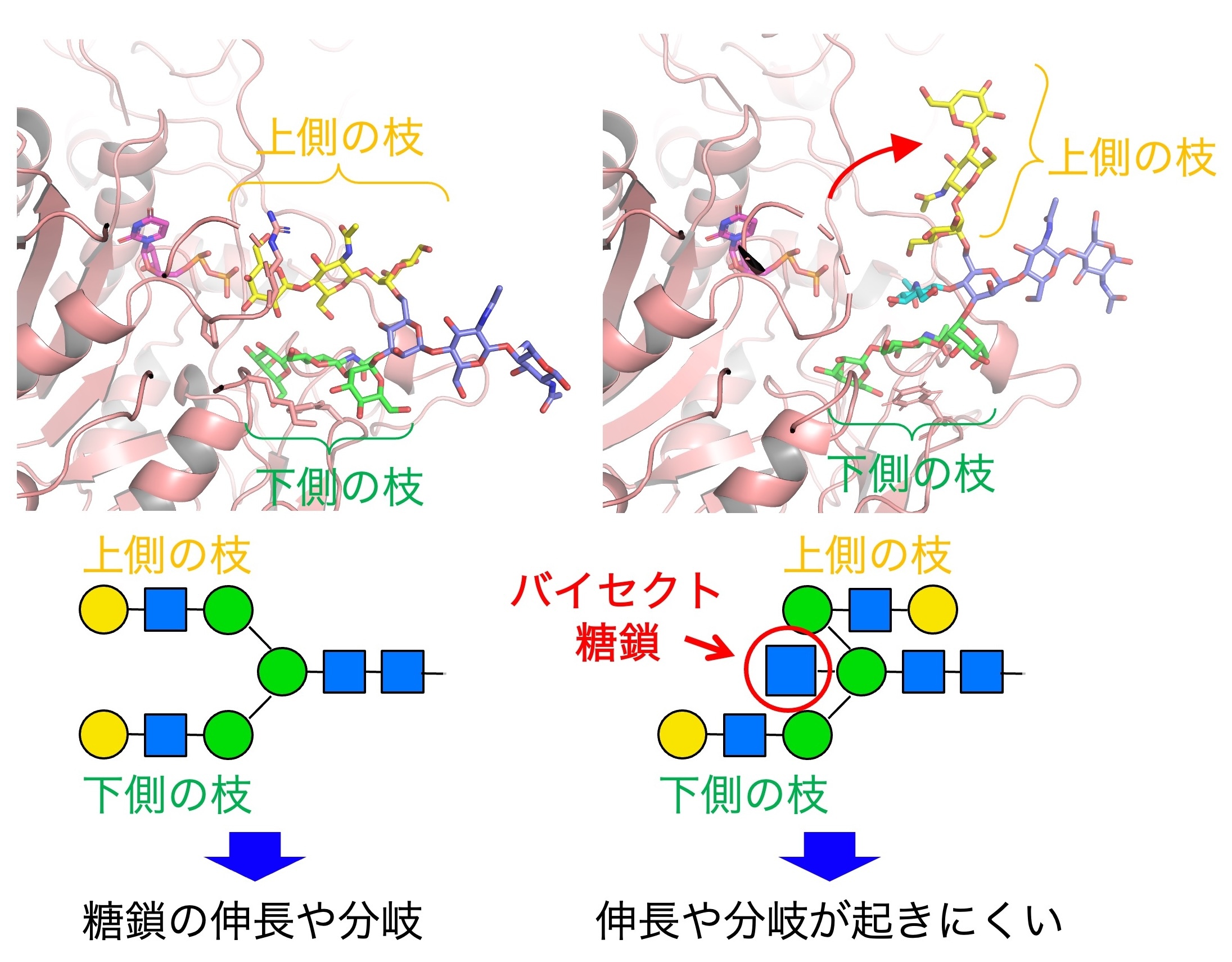
図3. バイセクト糖鎖があると、糖鎖の上側の枝の形が変化する。この変化によって、糖鎖の伸長やさらなる枝分かれなどが阻害され、複雑な糖鎖が作られにくくなる。
(参考文献:Nakano et al., Mol. Cell. Proteomics., 2019)
N型糖鎖の枝分かれ構造の一つに、バイセクト糖鎖(bisecting GlcNAc)という構造があります(図2上)。この枝分かれを持った糖鎖は、アルツハイマー病の発症や進行と深い関係があることがわかってきました。アルツハイマー病の原因はアミロイドβと呼ばれるペプチドが脳に蓄積することですが、この糖鎖を欠損したマウスでは、アミロイドβが作られなくなって症状が軽くなることがわかりました(図2下)。それは、アミロイドβを作る酵素であるBACE1がこの糖鎖を持っており、BACE1の機能がバイセクト糖鎖によって正に調節されているためです。さらに、アルツハイマー病の患者の脳ではバイセクト糖鎖の発現量が増加していることから、この糖鎖はアルツハイマー病の進行に関与することが示唆されています。しかし一方で、バイセクト糖鎖によってBACE1の機能が分子レベルでどのように調節されているのかその多くは謎のままです。 現在、この仕組みの解明に向けた実験やバイセクト糖鎖を合成する酵素MGAT3 (GnT-III)の立体構造の解析などを行っています。
またバイセクト糖鎖の持つ本来の生理機能についての研究も行っています。バイセクト糖鎖の3次元構造を調べたところ(図3)、通常の糖鎖と比較して、バイセクト糖鎖では糖鎖の上側の枝が反対方向に向きやすいことがわかりました(図3右)。通常は糖鎖がさらに伸長したり枝分かれしますが、バイセクト糖鎖では、この反転によりそのような伸長や枝分かれが起きにくいことがわかりました。つまり、バイセクト糖鎖ができることによって、複雑な糖鎖ができにくくなることから、バイセクト糖鎖はN型糖鎖全体の生合成を抑える働きがあることがわかりました。
現在、バイセクト糖鎖が高発現するニューロンや腎臓での役割を調べており、バイセクト糖鎖が腎臓での体液調節に重要な役割を果たすことを明らかにしました。またMGAT3の機能を調節するメカニズムなどについても研究を行っています。
がんを悪性化させるβ1,6分岐構造の研究
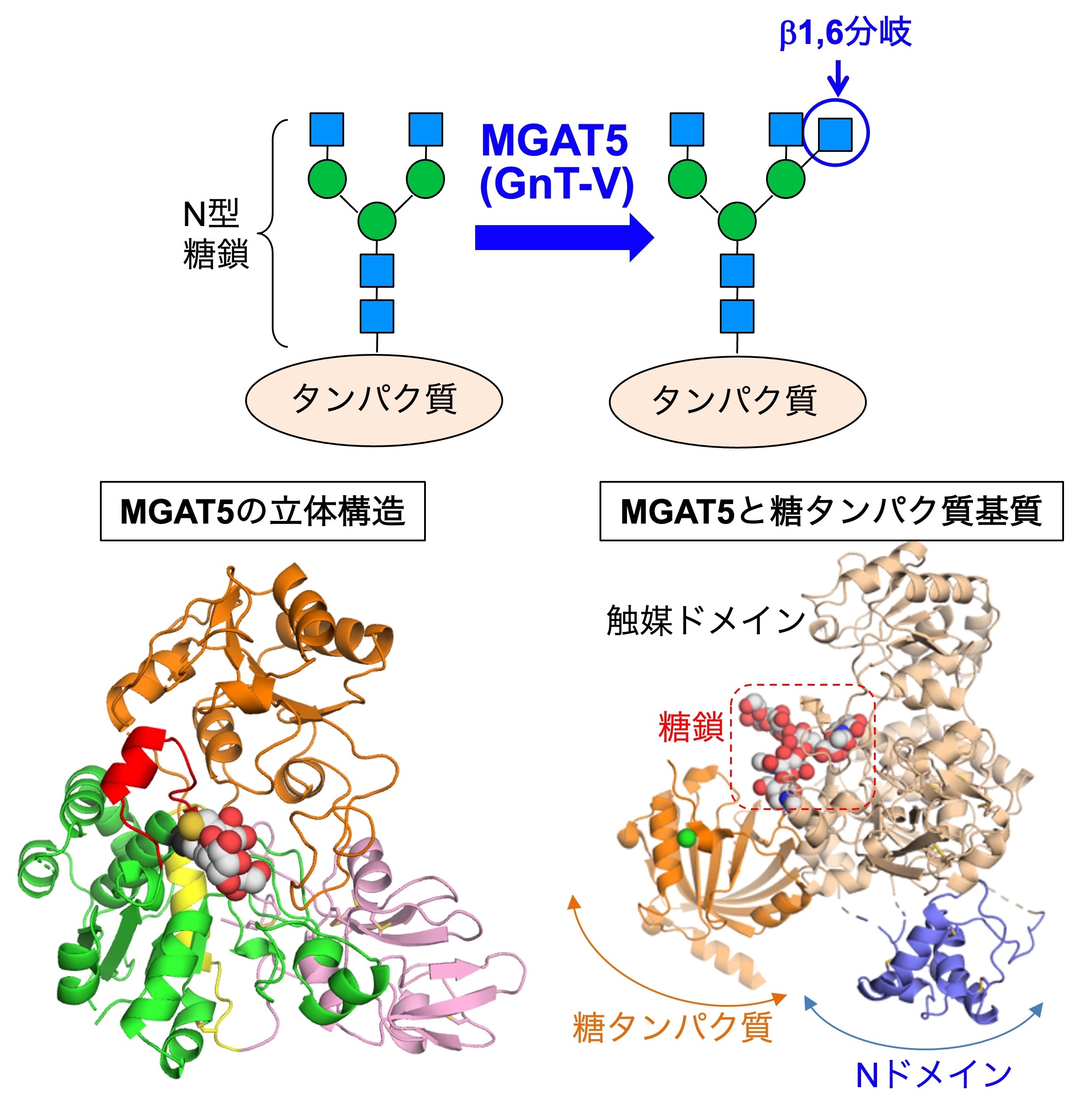
図4. (上) β1,6分岐構造と生合成酵素。(左下) MGAT5の立体構造。(右下)MGAT5と糖鎖修飾を受けるタンパク質とのドッキングモデル。
(参考文献:Nagae et al., Nat. Commun., 2018)
(参考文献:Osuka et al., J. Biol. Chem., 2022)
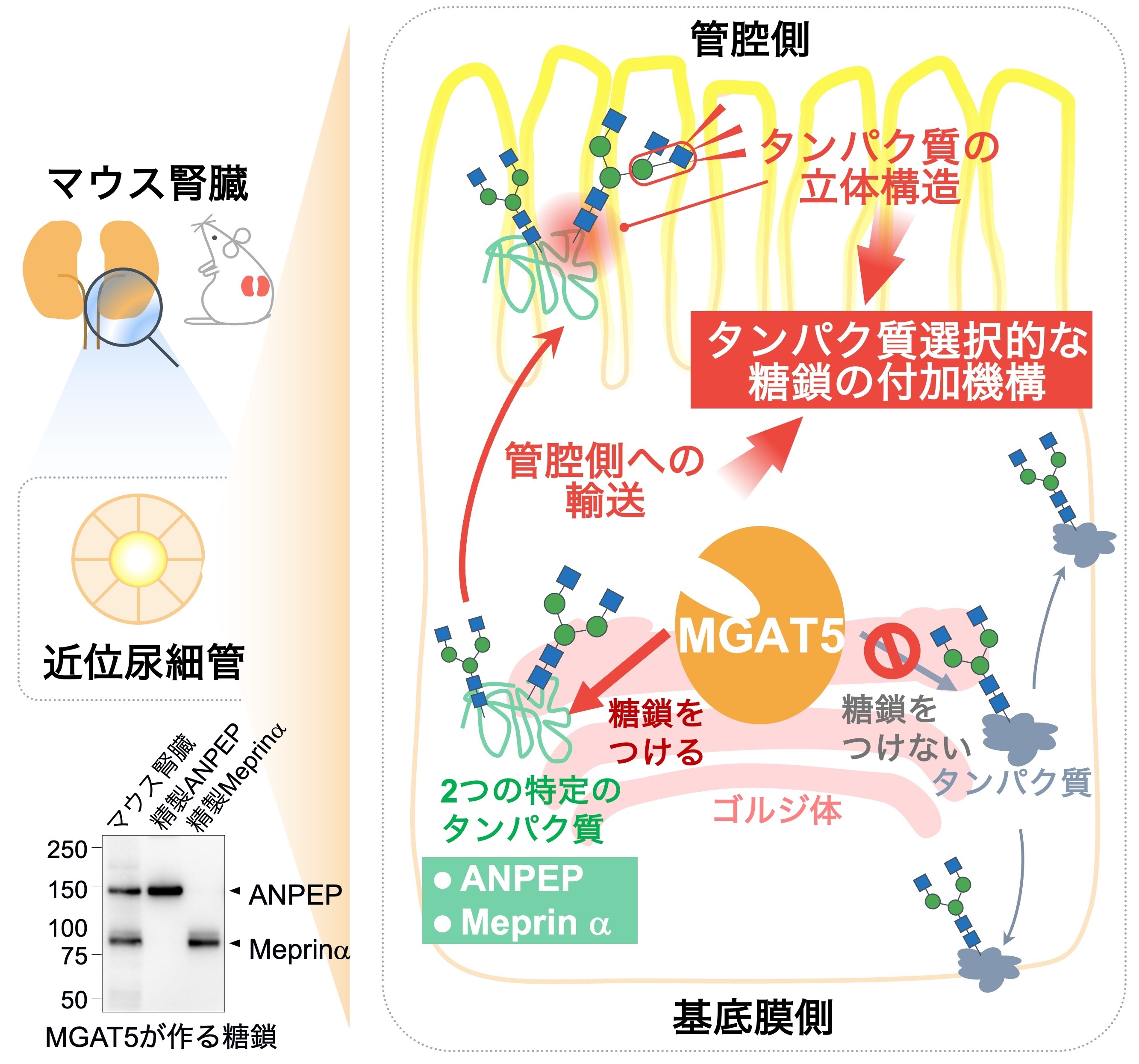
図5. 腎臓におけるMGAT5の基質糖タンパク質の選別とそのメカニズム
(参考文献:Osuka et al., iScience, 2025)
がんと関連の深いN型糖鎖の枝分かれ構造についても研究を行っています。特に、MGAT5 (GnT-V)と呼ばれる酵素が作るβ1,6分岐という枝分かれ構造は(図4上)、がんの増殖や転移を促進する働きがあることが以前から知られており、がんの創薬標的と考えられています。
私たちは、構造生物学の専門家(長江雅倫先生)と共同で、MGAT5の立体構造を世界で初めて明らかにしました(図4左下)。その結果、MGAT5がどのように糖鎖の形を認識してβ1,6構造を生合成するのか、そのメカニズムの基礎となる部分がわかってきました。この構造から、MGAT5に選択的な阻害剤の開発が進むことが期待され、実際に有機化学の専門家との共同でMGAT5の阻害剤の探索にも取り組んでいます。
一方で、細胞の中でMGAT5がどのように特定のタンパク質を選んで糖鎖を作っているのか、その詳細な分子メカニズムはまだわかっていません。その手がかりとして、MGAT5の中のNドメイン(図4右下)と呼ばれる領域が関わることがわかってきました。Nドメインを除いた変異体は、糖鎖に対する活性はほぼ完全に保持していたにもかかわらず、糖タンパク質に対する活性がほぼ消失していました。このことから、MGAT5はNドメインを介して糖タンパク質を認識する可能性が示されました。
また、MGAT5が糖鎖を付けるタンパク質をどのように選んでいるかを調べるため、MGAT5の活性が高いマウスの腎臓を用い、MGAT5が修飾するタンパク質を探索しました。その結果、近位尿細管の管腔側に存在する、ANPEPとMeprinαという2つのタンパク質がMGAT5によって主に修飾されていることがわかりました(図5)。これらの解析によって、マウス腎臓では、管腔側へのタンパク質の輸送やタンパク質の立体構造が組み合わさることで、MGAT5による修飾が起こることがわかりました。
現在は、MGAT5の機能が制御される仕組みの解明などに取り組んでいます。
糖尿病などに関わるMGAT4の研究
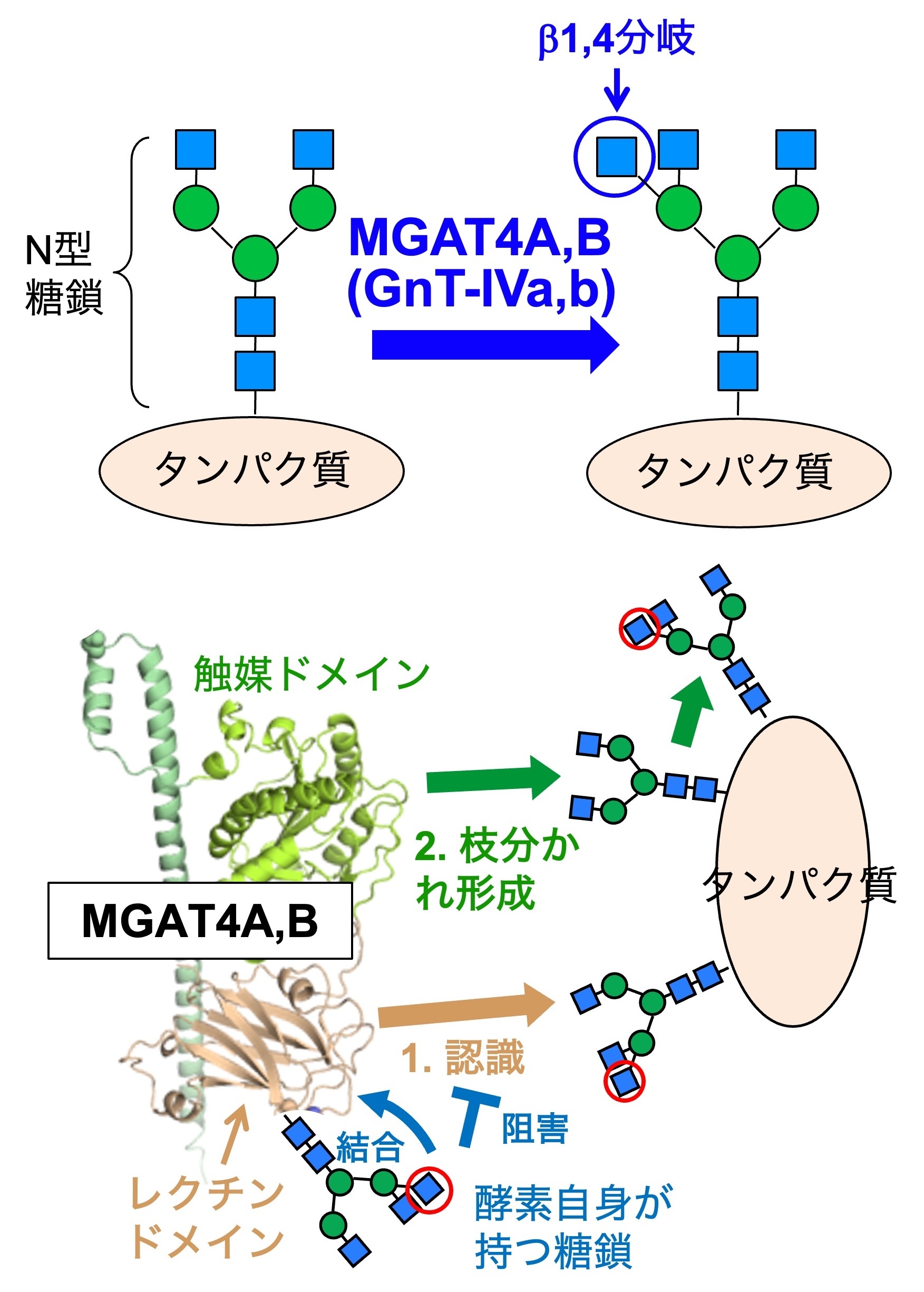
図6.(上) MGAT4Aと4Bが生合成するβ1,4分岐構造。(下) MGAT4A,Bは、糖鎖を作る触媒ドメインとは別に、糖鎖と結合するレクチンドメインを持っており、これによって基質タンパク質を認識して糖鎖を作る。さらに、酵素のレクチンドメイン自身にも糖鎖がついており、これがレクチンドメインの機能を阻害することで、活性を自己調節している。
(参考文献:Nagae et al., Commun. Biol., 2022)
(参考文献:Osada et al., J. Biol. Chem., 2022)
(参考文献:Osada et al., iScience, 2024)
さらに、糖尿病と関わるβ1,4分岐という枝分かれ構造についても研究を行っています。この枝分かれ構造は、MGAT4A (GnT-IVa)、 MGAT4B (GnT-IVb)という2種類の類似した酵素によって生合成されています(図6上) 。MGAT4Aを欠損するマウスでは膵臓の機能が低下し、血糖値が高まって糖尿病様の症状を呈することから、この枝分かれ構造は糖尿病などの治療標的となることが示唆されています。一方で、 MGAT4Aや4Bが細胞内においてどのような仕組みで糖鎖を作っているのか、またMGAT4Aと4Bという2つの類似した酵素の働きがどのように違うのか、ということについてはほとんどわかっていません。
最近私たちは、 MGAT4AやBが他の糖鎖合成酵素とは異なるレクチンドメインというものを持っていることを明らかにしました。さらにこのレクチンドメインは特定の糖鎖と結合し、これが触媒ドメインの糖鎖合成機能に不可欠であることがわかりました(図6下)。また、MGAT4AやBは、自分自身もレクチンドメインの中に糖鎖を持っており、この糖鎖が糖鎖構造依存的にレクチンドメインの機能を阻害していることから、MGAT4は自分自身の糖鎖で活性を自己制御していることがわかりました。N型糖鎖を作る酵素の中でこのような自己調節の仕組みを持つものは知られていないことから、MGAT4Aや4Bは全く新しい様式で糖鎖を作ることが示唆されました。
また最近では、MGAT4はA,Bだけでなく、C~Gまでが存在し、その遺伝子の数や各酵素の活性の有無が生物種間で大きく異なることを明らかにしており、MGAT4は種特有のN型糖鎖の枝分かれを合成するのに重要な役割を果たすことがわかりました。
COPDやがんに関わるコアフコースの研究
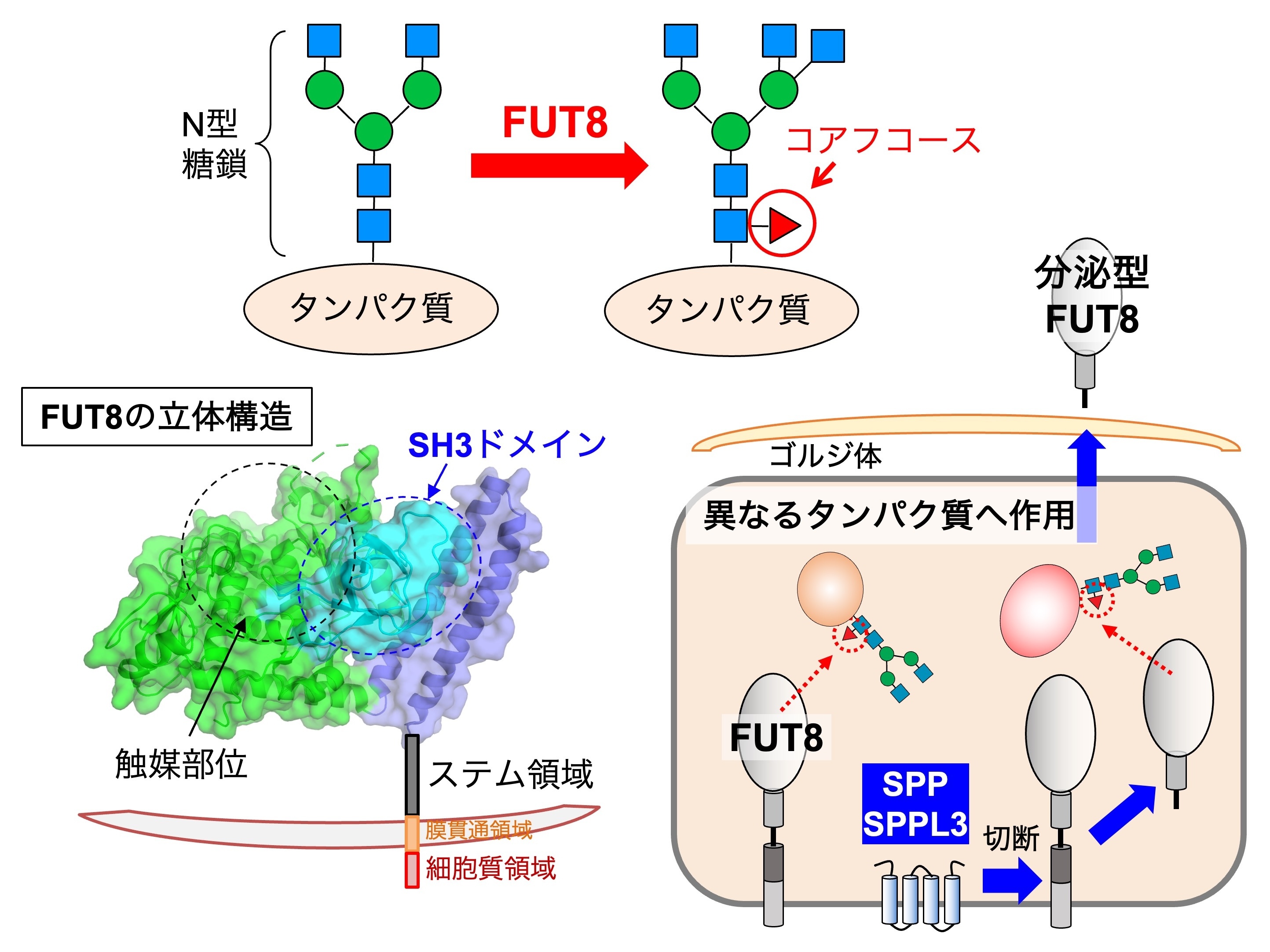
図7. (上) コアフコース構造と生合成酵素。(左下) FUT8の立体構造。FUT8は、触媒部位の他にSH3ドメイン、ステム領域などを持つ。(右下) FUT8はSPPやSPPL3により切断され、細胞外へと分泌される。この切断は、FUT8の基質タンパク質選択性を変化させる。
(参考文献:Tomida et al., J. Biol. Chem., 2020)
(参考文献:Tomida et al., J. Biol. Chem., 2022)
(参考文献:Tomida et al., J. Biol. Chem., 2026)
また、N型糖鎖の根元のコアフコースと呼ばれる枝分かれ構造についても研究を行っています。コアフコースは、FUT8と呼ばれる酵素によって作られ(図7上)、FUT8欠損マウスが肺気腫様の症状を呈することから、慢性閉塞性肺疾患(COPD)と関わることが知られています。また、コアフコースは肺がんや皮膚がんの増殖や転移を促進することも報告されています。さらに、抗体医薬品の糖鎖からコアフコースを取り除いて抗がん作用を100倍近く上昇させる技術が臨床現場で用いられるなど、コアフコースはこれらの疾患の診断や治療と深く関わっています。このようにコアフコースの重要な機能が明らかになりつつある一方で、コアフコースを作るFUT8の機能がどのように制御されているのかはまだあまりよくわかっていません。
私たちは、FUT8の立体構造や制御因子に着目して、FUT8の機能が細胞内でどのように制御されているのかを調べています。FUT8は立体構造がわかっており、糖鎖を合成する触媒部位の近傍に、他の糖転移酵素にはみられないSH3ドメインというユニークな領域を持ちます(図7左下)。このSH3ドメインは、FUT8の酵素活性に不可欠であり、またFUT8がRPN1と呼ばれるタンパク質と結合することにも必要であることがわかりました。また、FUT8のステム領域は、FUT8が多量体を形成するのに不可欠なことを明らかにしています。
さらに、FUT8はSPPやSPPL3などのプロテアーゼによって切断され、細胞外へ分泌されることがわかりました。この切断により、FUT8が作用する基質タンパク質の種類が変わることから、FUT8による細胞内での糖鎖修飾は、FUT8の切断分泌によっても制御されることが明らかになりました(図7右下)。
その他の糖鎖合成酵素の研究
脳機能と関連するO-マンノース型糖鎖の研究
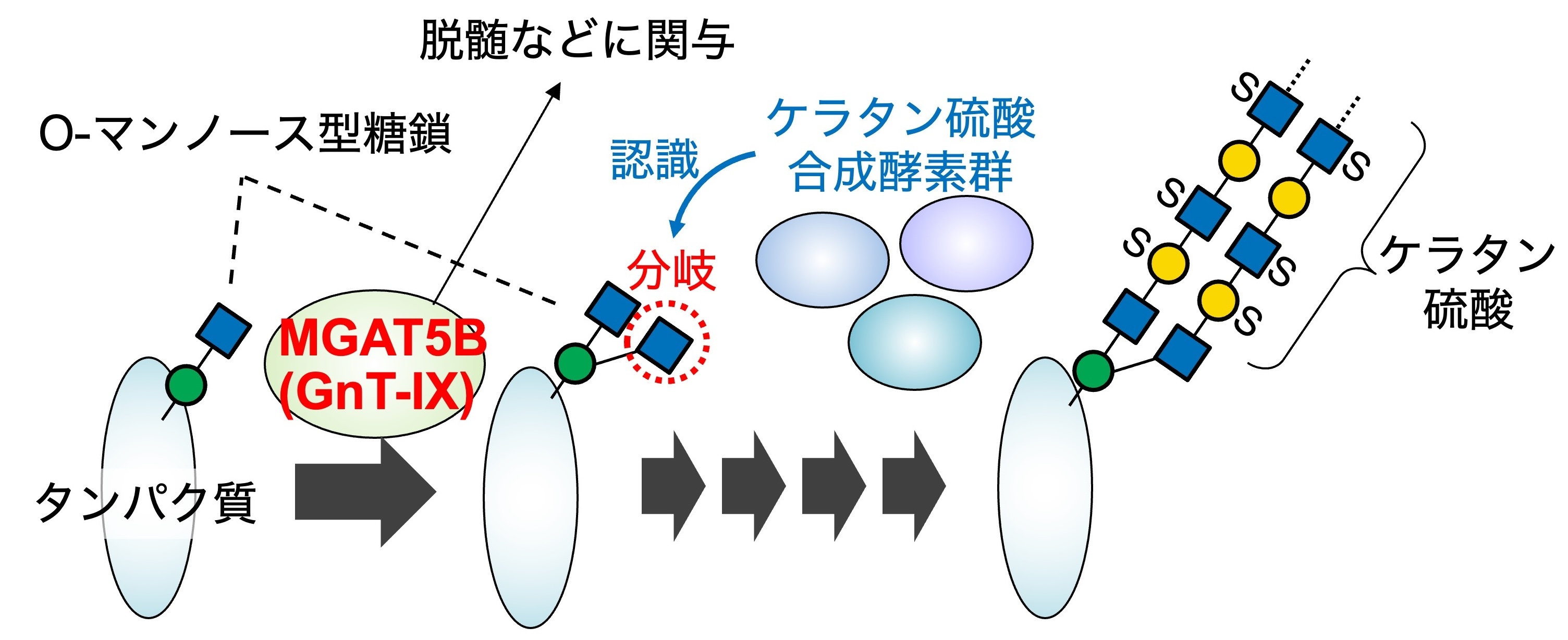
図8. MGAT5Bは脳特異的な糖転移酵素で、O-マンノース型糖鎖の枝分かれを作る。MGAT5Bにより枝分かれができると、それを他の酵素が認識して、ケラタン硫酸が糖鎖の先に作られる。
(参考文献:Itoh et al., J. Biol. Chem., 2026)
脳に特異的に発現し、脳の機能や脳疾患と関連するMGAT5B (GnT-IX)と呼ばれる酵素について研究しています。MGAT5Bは、O-マンノース型糖鎖の枝分かれを作る酵素で、脱髄疾患や脳腫瘍などに関わることがわかっています。私たちは、MGAT5Bが枝分かれを作ると、それを他の酵素が認識して、枝分かれしたO-マンノース型糖鎖の末端にケラタン硫酸と呼ばれる糖鎖構造が効率的に作られることを明らかにしました(図8)。また現在、MGAT5B欠損マウスを用い、分岐O-マンノース型糖鎖の脳における生理機能について調べています。
タンパク質の血中安定性やがんと関連するLacdiNAc糖鎖の研究
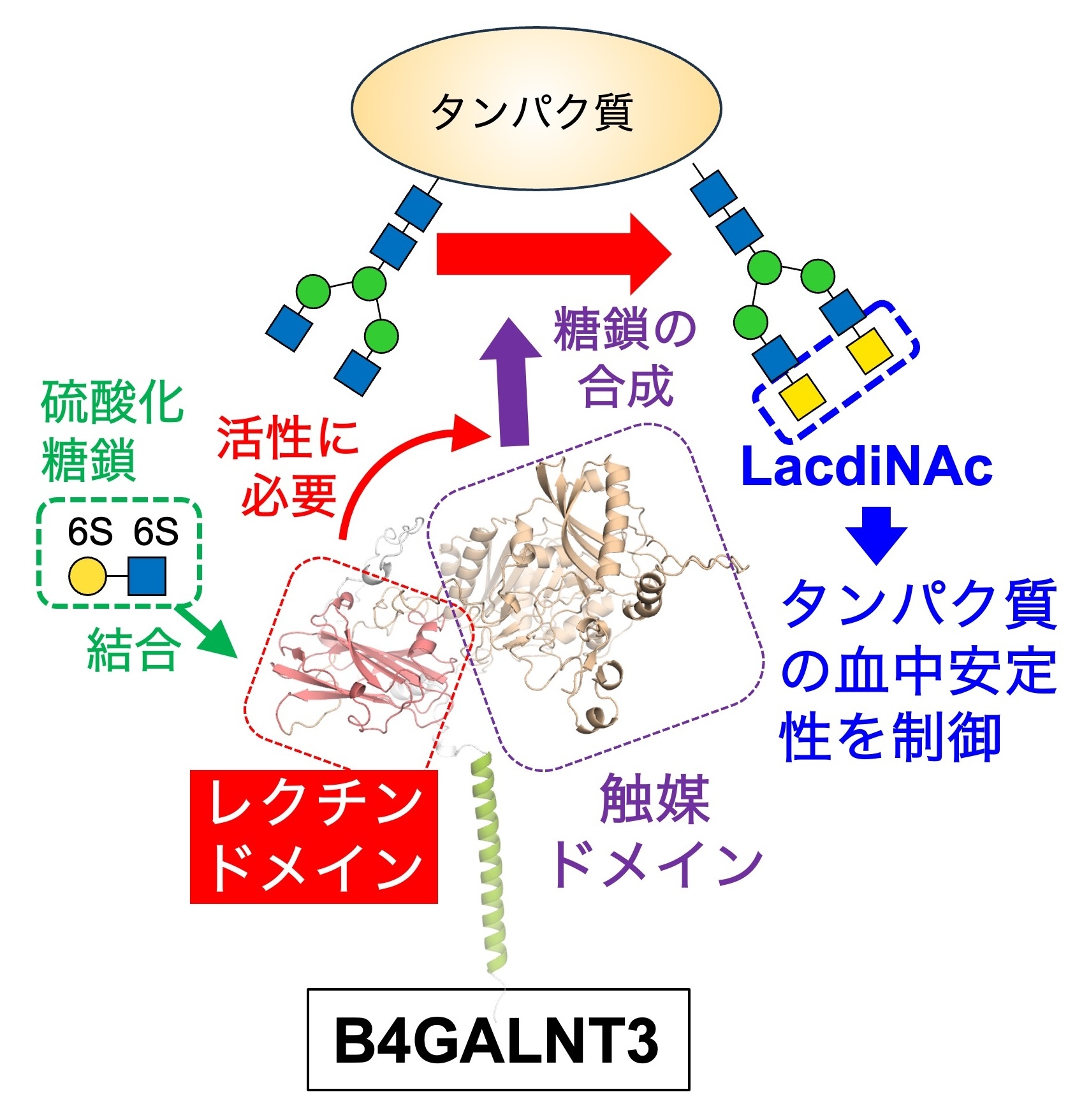
図9. B4GALNT3はLacdiNAcと呼ばれる糖鎖を作る糖転移酵素。最近、触媒ドメインの他に、活性に必要なレクチンドメインを持つことを明らかにした。
(参考文献:Tokoro et al., J. Biol. Chem., 2024)
(参考文献:Tokoro et al., J. Biol. Chem., 2026)
B4GALNT3と呼ばれる糖転移酵素のユニークな構造や機能について調べています。B4GALNT3は、LacdiNAcと呼ばれる、血中のタンパク質の安定性などを制御する糖鎖を合成します。この酵素の構造を調べると、触媒ドメインの他に、糖鎖と結合するユニークなレクチンドメインを持つことがわかりました。このレクチンドメインは、B4GALNT3が糖タンパク質に作用するのに必要であることや、硫酸化された糖鎖と結合することも明らかになりました(図9)。
また、B4GALNT3によりLacdiNAc構造が作られると、シアル酸やHNK-1などの末端構造の生合成が抑えられることから、B4GALNT3は糖鎖の成熟を抑制して構造を単純化させる働きがあることがわかりました。現在、B4GALNT3と疾患との関連性を調べています。
糖転移酵素の細胞内での活性調節の仕組みの研究
また、糖転移酵素の活性が細胞内で制御されるその他の様々な仕組みの解明に取り組んでいます。具体的には、糖転移酵素の局在制御、翻訳後修飾、複合体形成、分解、分泌などに着目した研究を行っています。
ヒト全糖転移酵素の活性情報の収集(HGA)
私たちは、文部科学省の大規模学術フロンティア促進事業が支援するプロジェクトの一つであるヒューマングライコームプロジェクト, (HGA)に参画しています。そこでは、糖鎖生合成アトラスの構築のため、ヒトの全ての糖転移酵素を収集し、その活性情報を基盤情報として取得します。得られた酵素活性の情報をプロジェクト内の他の情報と組み合わせることで、遺伝子発現から糖鎖発現を予測するシミュレーターの精度を上げることを目標にしています。
その他の研究テーマ
糖鎖の検出プローブや機能阻害剤の開発
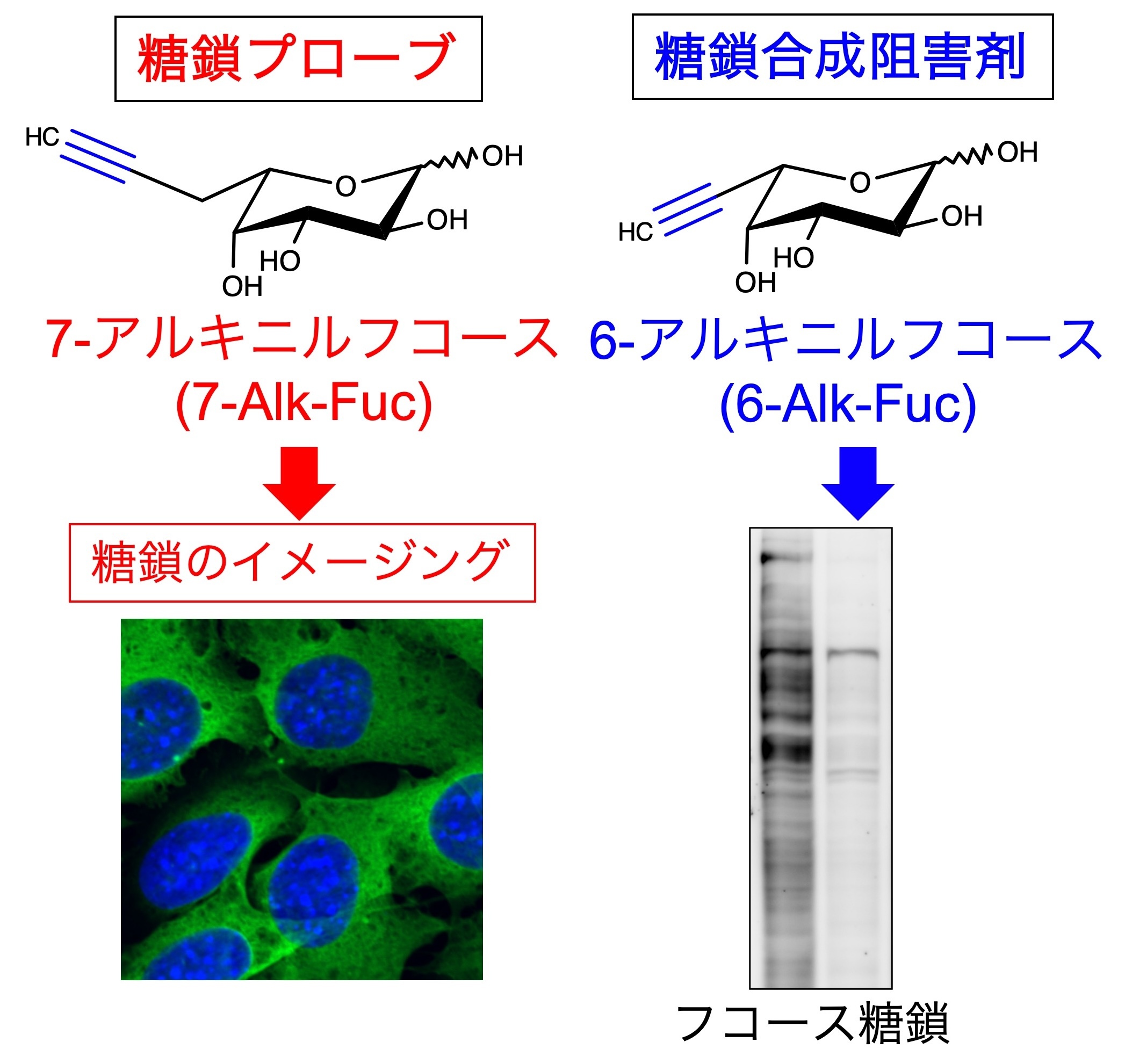
図10. 新しいフコースアナログによる糖鎖の検出と糖鎖合成阻害
(参考文献:Kizuka et al., Cell Chem. Biol., 2016)
(参考文献:Kizuka et al., Cell Chem. Biol., 2017)
糖鎖の研究をする上で、調べたい糖鎖を見ることは不可欠です。糖鎖を見るには、抗体やレクチンを使った手法が現在一般的ですが、私たちは、糖のアナログとクリックケミストリーを組み合わせて特定の糖鎖を検出する手法に着目しています(図10左)。それらのプローブを使った創薬標的の探索や疾患の診断マーカーの開発を目指しています。また、疾患の治療などの目的のため、特定の糖鎖の機能を阻害する化合物の開発も行っています。これまでに、フコース糖鎖の生合成を阻害してがん細胞の浸潤を抑える化合物の開発 (図10右)、岐阜大学の田中秀則先生らとの共同研究によるMGAT5の阻害剤候補の開発 (Vibhute et al., BBA Gen. Subj., 2022)、グリコサミノグリカンの生合成阻害剤の開発、などを行っています。
細胞外小胞 (sEV)と糖鎖に関する研究
細胞間の情報伝達の担い手として注目されるエクソソームなどの細胞外小胞(sEV)における糖鎖の組成や役割について、鈴木健一研究室 (iGCORE) と共同で研究しています。これまでに、がん関連糖転移酵素であるMGAT5ががん細胞由来のsEVに含まれ、それが受け手細胞に取り込まれることを明らかにしました(参考文献:Hirata et al., iScience, 2023)。また、神経特異的糖鎖であるHNK-1およびその生合成酵素B3GAT1 (GlcAT-P)もsEVに含まれており、HNK-1糖鎖も同様に細胞間を受け渡されることを見出しています(参考文献:Tokoro et al., J. Biol. Chem., 2026)。
GPI (Glycosyl Phosphatidyl Inositol) アンカーに関する研究
タンパク質に付加される糖脂質である GPI の生合成と機能について、特にプリオン病 や精神疾患との関連、また GPI アンカー型タンパク質の細胞内輸送などに関する研究 を行っています(参考文献:Hirata et al., J. Biol. Chem., 2022)。
アルギニンメチル化と糖鎖に関する研究
翻訳後修飾の一つとして知られるタンパク質のアルギニン残基のメチル化と、糖鎖・糖タンパク質の発現、機能の関係について、岐阜大学応用生物科学部の橋本美涼先生と共同で研究しています(参考文献:Hashimoto et al., BBA Gen. Subj., 2020)。
HNK-1 (Human Natural Killer-1) 糖鎖に関する研究
記憶・学習能力に不可欠な脳特異的糖鎖であるHNK-1の生合成の調節の仕組みについて研究しています。これまでに、MGAT3によってHNK-1の生合成が抑制されること、またそれは組織特異性があることなどを明らかにしています(参考文献:Kawade et al., Molecules, 2021)。
