研究内容
1.抗原・抗体複合体の分析技術開発
我々は、コロナウイルスなどの病原体や、害のある異物を排除するために複雑な免疫システムを備えていますが、抗体(免疫グロブリン)は液性免疫において特に重要なタンパク質です。抗体は、その標的(抗原)と結合し、抗原・抗体複合体を形成する事で、抗原の中和、他の免疫細胞への抗原の提示、抗体を介した細胞障害の誘導といった機能を発揮します。また抗原・抗体複合体は、液性免疫が関わる疾患(感染症・自己免疫疾患・癌など)の診断マーカーとしても利用されてきました。例えば、癌抗原に対する抗体は発癌後早期から血中で増加し、腫瘍組織中の免疫細胞の浸潤量や、癌免疫治療の効果、予後の良し悪しと相関することが知られています。 そのため様々な疾患で診断マーカーの開発を目指して、血液からの抗原・抗体複合体の精製と、複合体に含まれている抗原の同定が試みられてきました。しかし既存の精製法では、検体由来の夾雑物が十分に除去できておらず、高感度な抗原同定のボトルネックとなっていました。我々は、抗原・抗体複合体から抗原/抗体を高精度に分画させる独自システムを開発し、8倍以上の抗原同定を実現、特許出願を行いました(特願2022-152089, 下図)。 理論的には、抗体は約10億種類の多様性を持つと推定されており、抗原・抗体反応を丸ごと理解するためには、更なる分析技術の発展が必須です。我々は、免疫ゲノミクスとの統合や、免疫グロブリン種類ごと(アイソタイプ、サブタイプ)の精製技術、抗体機能を制御することが知られている糖鎖修飾情報との統合といった、多角的な観点から抗原・抗体複合体に関する分析技術の革新を目指しています。
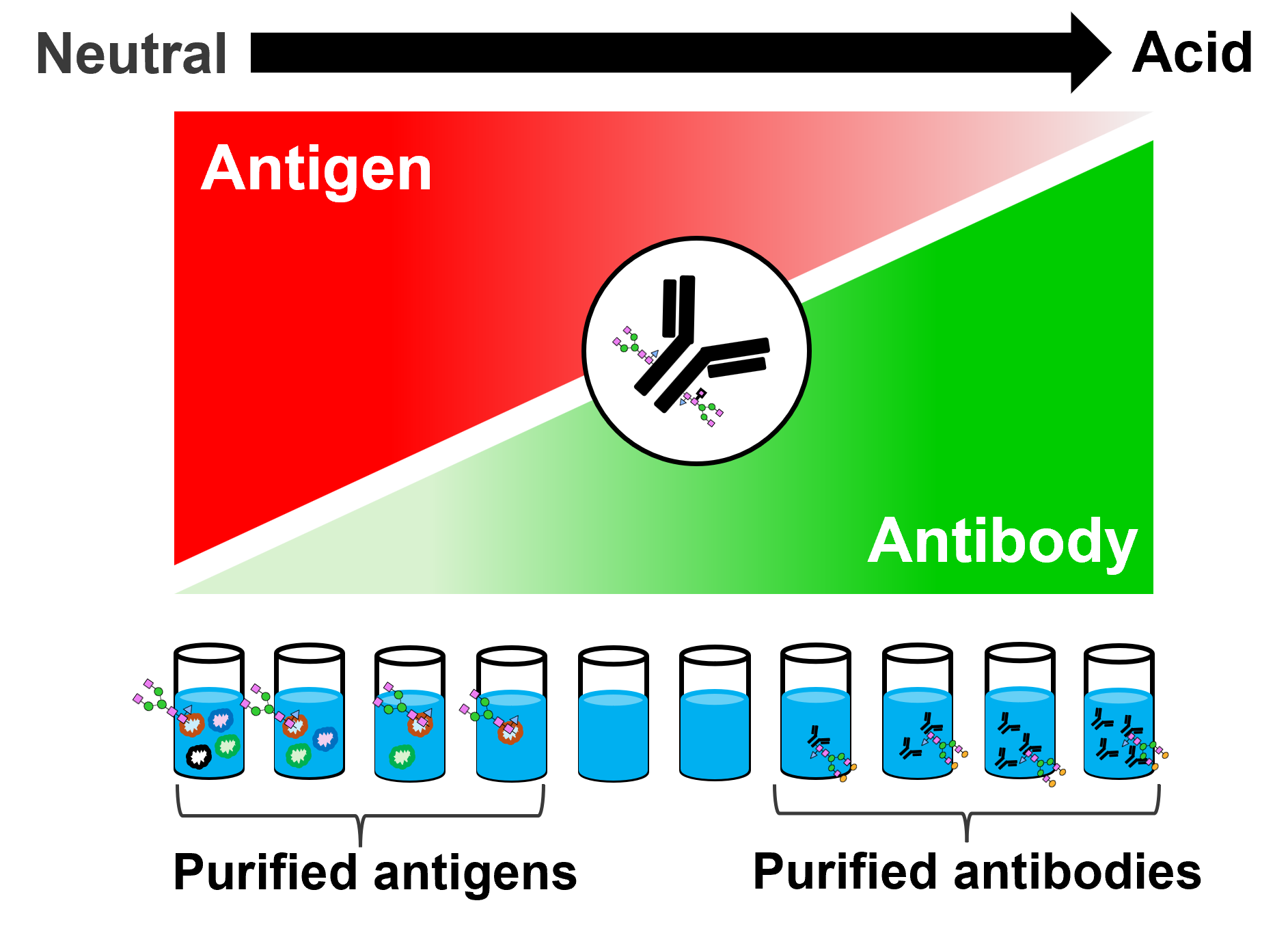
2.時空間的な抗原・抗体複合体の形成メカニズムの理解
これまでの抗原・抗体複合体研究では、診断マーカーとしての応用の観点から、血液検体を中心とした解析が進んできました。一方で、腸管や腹腔中にも多量の抗体が分泌され、液性免疫応答に関与しています。特に重要な点として、分泌される場所ごとに異なるタイプのB細胞が存在し、血中(B2細胞)では免疫グロブリンG1、腸管・腹腔(B1細胞)では免疫グロブリンA・免疫グロブリンG3あるいはMが、それぞれ異なる抗原・抗体反応を制御し、液性免疫応答の中心を担うと考えられてきました(下図)。 近年、老化あるいは自己免疫疾患の進行に伴い、特に腹腔内で抗体のレパートリーが変化する事が、免疫ゲノミクスにより明らかとなりつつあります。一方で、どのような組み合わせの抗原・抗体複合体が腹腔内に存在しているのか、また抗体上の糖鎖修飾がその制御にどう関与するか、理解は進んでいません。我々は、独自の分析技術により、時空間的な抗原・抗体複合体の分析、特に腹腔内における液性免疫応答の理解を目指しています。

