僈僗僴僀僪儗乕僩
僈僗僴僀僪儗乕僩偺峔憿
僈僗僴僀僪儗乕僩偼悈曪愙壔崌暔偲傕屇偽傟丄悈慺寢崌偵傛傞悈暘巕偺僇僑忬峔憿偺拞偵懠偺暔幙偺暘巕偑擖傝崬傫偩傕偺偱偡丅偙偺暔幙偼儊僞儞乮CH4乯僴僀僪儗乕僩傗擇巁壔扽慺乮CO2乯僴僀僪儗乕僩偵戙昞偝傟傞傛偆偵崅埑椡壓偱惗惉偡傞摿挜偑偁傝傑偡丅埲壓偱愭偢僈僗僴僀僪儗乕僩偺峔憿偵偮偄偰娙扨偵愢柧偟傑偟傚偆丅
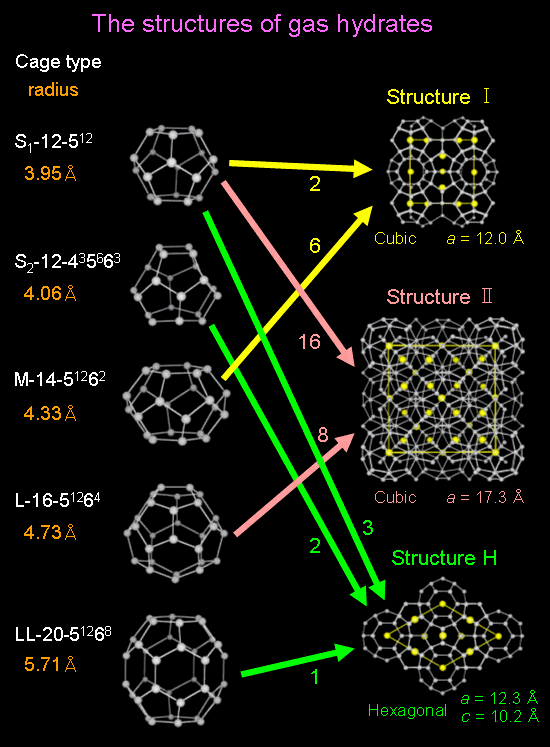
僈僗僴僀僪儗乕僩偼壓偺恾偵帵偡傛偆偵戝偒偔暘偗偰 峔憿嘥乮Structure I乯丄峔憿嘦乮Structure II乯丄峔憿H乮Structure H乯 偺3偮偺峔憿偵戝暿偝傟傑偡丅峔憿嘥偼2偮偺12柺懱乮S1働乕僕乯偲6偮偺14柺懱乮M働乕僕乯偐傜側傞棫曽徎丄峔憿嘦偼16屄偺12柺懱乮S1働乕僕乯偲8偮偺16柺懱乮L働乕僕乯偐傜側傞棫曽徎丄峔憿H 偼3偮偺12柺懱乮S1働乕僕乯偲宍忬偺堎側傞12柺懱乮S2働乕僕乯2偮偲戝偒偄1偮偺20柺懱乮LL働乕僕乯偐傜側傞榋曽徎偱偡丅 奺働乕僕偼悈暘巕偵傛傝峔惉偝傟乮悈暘巕偼悈慺寢崌偵傛傝寢崌乯偙傟傜儂僗僩働乕僕偺拞偵尨懃1偮偺僎僗僩暘巕乮偨偲偊偽CO2傗CH4偺暘巕乯偑晻偠崬傔傜傟偰偄傑偡丅 傑偨丄峔憿偺堘偄偼僎僗僩暘巕偺戝偒偝偵埶懚偡傞偲偄傢傟丄椺偊偽僎僗僩暘巕偑 CO2丄CH4 偺応崌偼峔憿嘥偺僴僀僪儗乕僩傪丄N2丆O2丆Ar 偺応崌偵偼峔憿嘦偺僴僀僪儗乕僩傪惗惉偟傑偡丅

忋婰働乕僕偺僌儗乕偺娵偼巁慺尨巕傪丄僌儗乕偺朹偼悈慺寢崌傪昞偟偰偄傑偡丅 悈慺尨巕偼奺巁慺尨巕娫偵1屄偢偮懚嵼偟傑偡丅峔憿嘥丆嘦丆H 拞偺墿怓偺娵偼僎僗僩暘巕傪昞偟偰偄傑偡丅
僈僗僴僀僪儗乕僩偺扨寢徎嶌惉
丂 愭偵怗傟偨傛偆偵丄僈僗僴僀僪儗乕僩偼崅埑椡壓偱惗惉偟傑偡丅偦偙偱丄僟僀儎儌儞僪丒傾儞價儖丒僙儖偵悈偲僎僗僩乮僈僗乯暘巕帋椏傪晻擖偟丄怲廳偵埑椡偲壏搙傪惂屼偟側偑傜扨寢徎傪嶌惉偟傑偡丅変乆偺尋媶幒偱幚嵺偵嶌惢偟偨 CH4僴僀僪儗乕僩偲 CO2僴僀僪儗乕僩偺扨寢徎幨恀傪壓偵帵偟傑偡丅
| 儊僞儞僴僀僪儗乕僩扨寢徎 乮23亷丆栺200婥埑乯 |
擇巁壔扽慺僴僀僪儗乕僩扨寢徎 乮16亷丆栺5000婥埑乯 |
偙偺傛偆偵偟偰嶌惢偟偨扨寢徎帋椏偵懳偟偰丄崅埑儔儅儞丒僽儕儏傾儞嶶棎暘岝應掕傪峴偄丄僈僗僴僀僪儗乕僩偺暘巕僟僀僫儈僋僗丄埑椡桿婲峔憿憡揮堏丄抏惈揑惈幙丄峔憿埨掕惈傪挷傋抧媴娐嫬僄僱儖僊乕栤戣偵峷專偟偰偄傑偡丅
擱偊傞昘夠乽儊僞儞僴僀僪儗乕僩乿
丂儊僞儞乮CH4乯僴僀僪儗乕僩偼悈怺 500 m 埲壓偺擔杮嬤奀乮撿奀僩儔僼丄摍乯偺奀掙偵戝検偵杽憼偝傟偰偍傝丄偦偺検偼擔杮偺揤慠僈僗偺擭娫徚旓検偺100攞埲忋偲傕偄傢傟丄愇桘帒尮偵懼傢傞怴僄僱儖僊乕偲偟偰拲栚偝傟偰偄傑偡丅壓偺幨恀偼変乆偺尋媶幒偱崌惉偟偨CH4僴僀僪儗乕僩傪擱從偝偣偰偄傞條巕偱偡丅幨恀傪僋儕僢僋偡傞偲擱從偡傞條巕傪價僨僆(mpeg1, 1,329 kb, 姶扱偺惡擖傝丠)偱尒傞偙偲偑偱偒傑偡丅乮尒傟側偐偭偨傜偛傔傫側偝偄丅乯